| Мова : |
|
| Енциклопедія співтовариство |Енциклопедія відповіді |Відправити запитання |Словник знань |Завантажити знання |
Аміак |
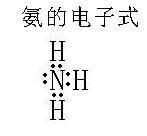 |
|
Технологія Визначення Китайська назва: Аміак Англійська назва: аміак Визначення: MF як "NH3", 4 атомів.Прикладна наука: Астрономія (об'єкта); міжзоряних молекул (два суб'єкта) Вище утримання Національного комітету науки і технологій оголосив затвердження Аміак (аміак, тобто аміак), або "аміак" формула NH3, являє собою безбарвний газ з сильним їдким запахом. Легко розчинний у воді при кімнатній температурі і тиску обсяг водорозчинного 700 разів більше обсягу аміаку. Аміак істот на Землі дуже важливо, все це є важливим компонентом харчування і добрива. Всі препарати аміак утворюється безпосередньо або побічно. Аміак має дуже широкий спектр застосування, але він також має корозійно небезпечним характером. Через широкого діапазону застосувань аміаку, аміак є найбільшим світового виробництва неорганічних сполук, більше ніж вісімдесят відсотків аміак використовується для виготовлення добрив. Аміак може бути надана як неподіленої пари електронів, також підставою Льюїса. Короткий вступ Аміак: [AN] [ㄢ ˉ] (іон амонію: NH 4 ) Чжен код: MYWZ, U: 6C28, ГБК: B0B1 Wubi: RNPV Висота підйому: 10, радикальний: газ, напівзакриті структури хід число: 3115445531 Посилання Глосарій: Англійська: аміак (аміак) Хімічна формула: NH3 Електронне: як право По-перше, структура: аміак молекули Ерленмейера молекула є полярною молекули. N атомів sp3-гібридні орбіталі. По-друге, фізичної природи: аміак при нормальних умовах являє собою безбарвний газ з різким запахом, меншу щільність, ніж повітря, легко розчинний у воді, легко скраплений аміак може бути використаний в якості холодоагенту. Розчинність розчинний у воді з 700:1. Молярна маса: 17.0306g/mol CAS: 7664-41-7 Щільність: 0,6942 Температура плавлення (МП): -77,73 ° C Точка кипіння (АТ): -33,34 ° C Критична точка: 132,9 ° C, 11.38MPa 25% ~ 28% концентрованого водного розчину аміаку Щільність: 0,899 г / мл, від 0 ° C Межа вибуховості: 15,8% -28% Дипольний момент: 1,42 D Основними хімічними властивостями 1, NH3 (летючих) у разі HCl (летючих) виробляє білі димові гази можуть вступати в реакцію з хлором. 2, аміак (водний аміак, NH3 · H2O), які схильні до корозії багатьох металів, зазвичай завантажуються з залізом, якщо аміак, залізо має бути в межах асфальтового покриття. 3, каталітичне окислення аміаку є екзотермічної реакцією, продукт NO є важливим промислового виробництва азотної кислотою реакції, NH3 може бути окислений до N 2. 4, NH3 зробити вологе червоною синьою лакмусового папірця. У воді виробляє невелику кількість гідроксильних іонів, слабо лужний. ⒌ аміак реагує з кислотою амонію: NH3 HCI = NH 4 Cl |
| Користувач Огляд |
|
Немає коментарів |