| Мова : |
|
| Енциклопедія співтовариство |Енциклопедія відповіді |Відправити запитання |Словник знань |Завантажити знання |
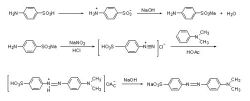
Диазотирование |
 |
|
Ароматичні первинне дію амін і нітрит (у кислому середовищі) з утворенням діазоніевой солі реакції діазотування позначений (зазвичай при низькій температурі, первинного аміну і кислоти співвідношення моль: 1:2,5), широко відомий ароматичний первинний амін діазо-компонента, нітрит диазотирования агент, азотистої кислотою є нестабільним, оскільки, як правило, нітрит натрію і соляна кислота або сірчана кислота, яка утворюється при реакції з ароматичним первинним аміном нітрит реагує негайно, щоб уникнути розкладання азотистої кислоти, диазотирования Після реакції солі діазонію.Основна інформація Диазотирование діазо-реакцію Наприклад, аліфатичні, ароматичні та гетероциклічні первинних амінів може здійснюватися диазотирования. Як правило, диазотирования реагент нітриту натрію і соляної кислоти генерується тимчасовий. На додаток до соляна кислота, можна використовувати сірчану кислоту, хлорне кислоту та інші неорганічні кислоти і фтор. Дуже нестабільний аліфатичні солі діазонію, може швидко розкладаються спонтанно, ароматичні солі діазонію є більш стабільним. Ароматичні групи диазония можуть бути заміщені іншими групами, щоб генерувати різні типи продукту. Таким чином, диазотирования ароматичних дуже важливо в органічному синтезі. Механізм реакції діазотування є першою комбінацією аміну з диазотируются агентом, а потім через серію перенесення протона, і, нарешті генерувати діазоніевой солі. Диазотирование реагенти, використовувані у формі неорганічних кислот і відповідних. При слабкої кислоти азотної кислоти в розчині з триоксида діазоту для досягнення збалансованого та ефективного диазотирования агент закис азоту. При сильної кислоти протоніруется диазотирования агент азотистої кислотою і нітрозільних позитивних іонів. Таким чином, реакції діазотування, належний контроль рН має важливе значення. Слабкі лужної первинний ароматичний амін, місцями реагент нітрозірованія необхідності, як правило, здійснюється в сильних кислої реакції. Ароматичні первинний амін і нітрит реагує з діазоніевой солі відзначений як реакції діазотування, яку часто називають ароматичним первинним аміном діазо-компонента, нітрит диазотирования агент, азотистої кислотою є нестабільним, оскільки, зазвичай нітрит натрію і соляної кислоти або сірчаною кислотою, азотною кислотою утворюється, коли реакцію з ароматичним первинним аміном негайно, щоб уникнути розкладання азотистої кислоти, реакції діазотування солі діазонію. Формула Диазотирование реакція може бути виражена як: Ar-NH 2 NaNO2 2HX --- Ar-N2X NaX 2Н20 Фактори Кількість кислоти У реакції діазотування, роль неорганічних кислот є: спочатку зробити ароматичний амін розчиняють з подальшою генерації нітриту і нітрит натрію, і, нарешті, вступає в реакцію з ароматичним діазоніевой солі амінів. Розкладання діазоніевой солі, як правило, легко, і тільки в надлишком кислоти в тільки відносно стабільною. Таким чином, навіть у відповідності з розрахунками реакційної схемою, тертя терти тільки дві амінокислоти диазотирования кислоту; Але для протікання реакції, кислота повинна бути належним чином передозування. Надлишок кислоти залежить від ароматичних лужної амін. Лужні слабкіше, чим більше надлишок, зазвичай більше 25% -100% перегодуєте більше, і навіть бути концентрованої сірчаної кислоти. Якщо реакції діазотування менше кількості кислоти і отриману сіль діазонію легко і непрореагировавшего ароматичного аміну з'єднання диазония аміносполуки. Це є незворотнім самостійно реакції сполучення, яке погіршує якість солі діазонію, впливає на нормальну реакції поєднання і знижує вихід цільового з'єднання. У разі недостатньої діазоніевой солі кислоти легко розкладається, і чим вище температура, тим швидше відбувається розкладання. Генеральний реакції діазотування завершено, розчин ще називають сильною кислотою, може Конго червоним кольором паперу. Концентрація кислоти Концентрація неорганічних кислот диазотирования ароматичних амінів ніколи не розчиняється розчинної солі амонію, солі амонію розчинений у вільному нітрит гідроліз іонізації аміну і обговорюється декілька аспектів. Дозування HNO2 За рівняння реакції діазотування, 1 моль диазотирования потрібно 1 моль нітриту натрію. Диазотирование проводиться, повинна підтримуватися протягом невеликого надлишку нітриту натрію, або причиною самостійного реакції сполучення. Це може бути, щоб керувати швидкістю нітриту натрію. Швидкість подачі занадто повільно, не диазотирования ароматичних амінів і роль діазоніевой солі реакції сполучення відбулися с. Написано нітрит розкладання відбувається занадто швидко, або інших побічних ефектів. Доступно при реакції крохмалю - калій йодид індикаторний папір для визначення у відповідності з різними квітами. Надлишок нітриту також є несприятливим для наступного муфта, з'єднувальний компонент буде нітрозірованія, окислення або інших реакцій. Таким чином, після реакції додати сечовини або сульфамінової кислотою розкладання надлишку нітриту. Температура реакції Диазотирование реакцію зазвичай проводять при температурі 0-5 ℃, солі діазонію Це тому, що найбільш стабільними при низьких температурах, при більш високих температурах, розкладання швидкість диазония результати солі. Також при більш високих температурах нітрити легко розкладається. Диазотирование температура реакції зазвичай залежить від стабільності солі діазонію, - висока стабільність сульфаниловой кислоти діазоніевой солі, диазотирования температури може бути здійснено при 10-15 ℃; 1 - амінонафталін-4 - сульфокислота вага більш високу стабільність азоту солі, диазотирования температура може бути в 35 ℃. Диазотирование Реакцію зазвичай проводять при більш низькій температурі принцип не є абсолютним, діазореакція в горщику періодичної реакції протягом тривалого часу, підтримання низької температури реакції правильно, але в трубопровід для диазотирования, реакція солі діазонію генерується в перерахунку скоро, так що реакції діазотування при більш високих температурах. Ароматичні аміни лужної Див механізму реакції, тим сильніше лужної ароматичні аміни, більш сприятливою N-нітрозірованія диазотирования тим самим збільшуючи швидкість реакції. Однак в сильно основних амінів з сіллю амонію кислота знижує концентрацію вільного аміну, таким чином, він також інгібує швидкість реакції діазотування. При концентрації кислоти є низькою, ароматичний амін N-нітрозірованія основний право основний вплив, то сильніше лужної ароматичні аміни, швидкість реакції швидше. При високій концентрації кислоти, солі амонію гідроліз основне питання факторів складності, то менше основний диазотирования ароматичних первинного аміну високою швидкістю. Загальний підхід Метод диазотирование і метод зворотного завдання по Франції двома способами. Знаєш що? Згладжування Згладжування в кольорі до додавання відповідної кількості води змішують, потім додають необхідну кількість соляної кислоти, при низькій температурі і при постійному перемішуванні повільно додають нітрит натрію, реакції діазотування завершена. Хромофора червоно G, і GC базовий колір помаранчевого кольору фіолетовий соусом база може бути використана поряд GBC методом. Диазотирование температура 5 ~ 10 ℃, протягом приблизно 10 хвилин, температури, часу надто мало, диазотирования не можете отримати кращий результат. Щоб диазотирования реакція завершена, необхідно помістити диазотирования колір розчину основи 15 хвилин або близько того, перед використанням додати потрібну кількість оцтової кислоти і ацетату натрію. Більшість розчинних у розбавлених мінеральних кислот, ароматичних первинний амін диазотирования з використанням цього методу. Метод зворотної Зворотні базовий колір диазотируют з нітритом натрію та відповідної кількості води в однорідну пасту і охолодженні льодом, а потім повільно виливають у суміш льоду з постійним перемішуванням розчин соляної кислоти, реакція була завершена, червоний колір групи B, диазотируют використанням методу зворотного завдання. Нерозчинні в розведеною кислоті аміно-ароматичних сульфокислот метод диазотирования кислота була застосована. HNO5S Франції Нітрозільние сірчаної кислоти методом, використовуваним в розбавлену кислоту нерозчинними ароматичним первинним аміном (лужні дуже слабка) диазотированного ароматичним первинним аміном спочатку розчиняють в концентрованої сірчаної кислоти або оцтової кислоти, додатково включає додавання натрію нітроксильних розчину сірчаної кислоти. Інші методи |
| Користувач Огляд |
|
Немає коментарів |